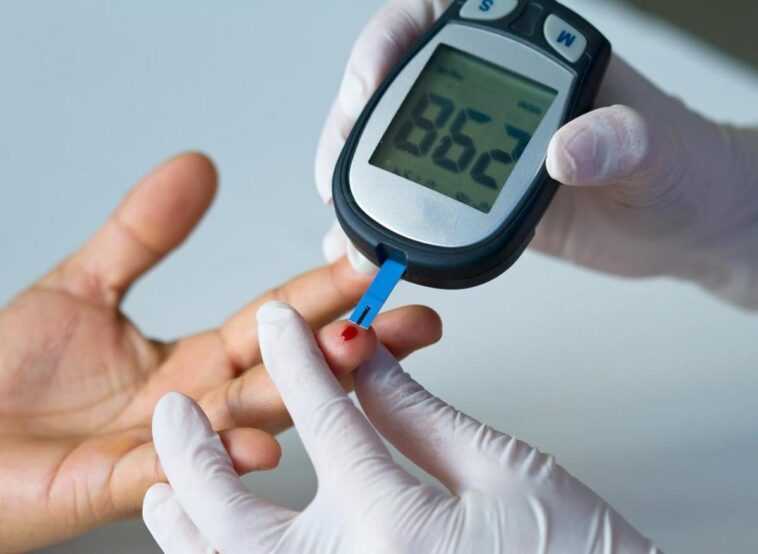
Il s’agit du teplizumab, un médicament d’immunothérapie qui agit en s’attaquant à la cause de la maladie, plutôt qu’aux seuls symptômes.
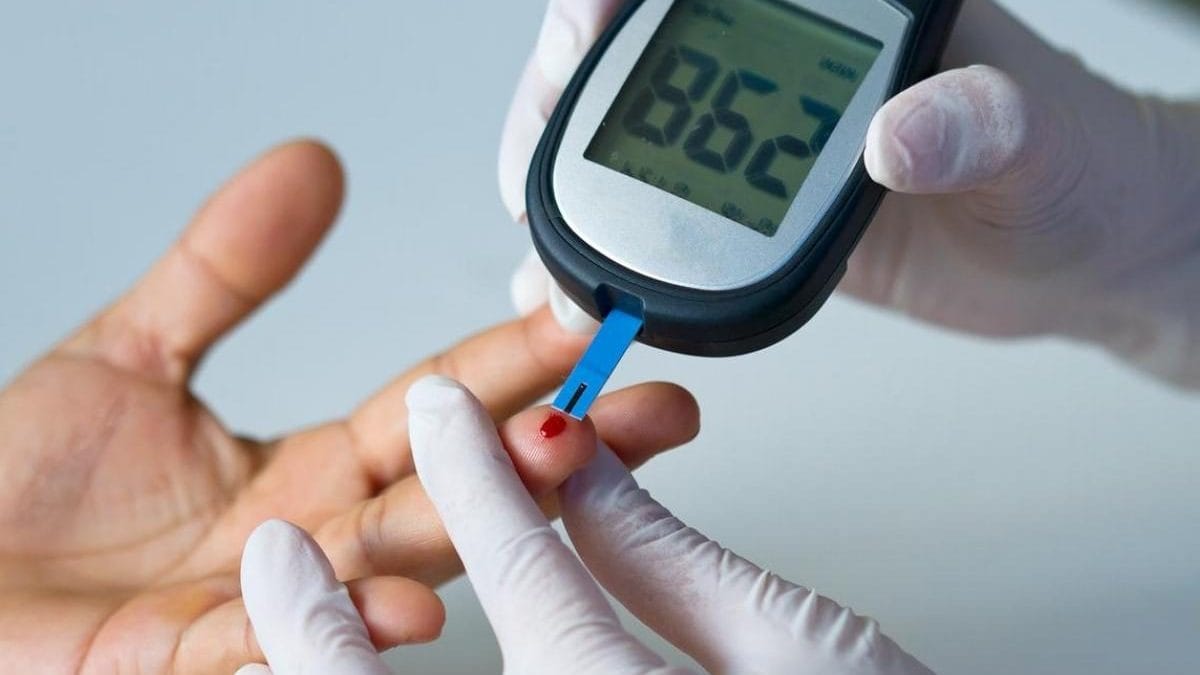
Un médicament révolutionnaire, dont il a été démontré qu’il retardait le développement du diabète de type 1, a été approuvé par les autorités de réglementation américaines, marquant une nouvelle ère dans le traitement de cette maladie auto-immune. Il s’agit du teplizumab, un médicament d’immunothérapie qui agit en s’attaquant à la cause du diabète de type 1, qui peut être très important, en particulier pour les patients plus jeunes, qui peuvent éviter de prendre de l’insuline tous les jours et surveiller régulièrement leur glycémie dans le sang.
Bien que le diabète de type 1 puisse survenir à tout âge, il est principalement diagnostiqué chez les enfants et les jeunes adultes. Et c’est pour cette raison qu’on l’appelle aussi diabète infantile, bien que le diabète de l’adulte ne soit pas rare. La maladie est causée par la production d’auto-anticorps qui attaquent et détruisent les cellules bêta du pancréas, responsables de la production d’insuline, ce qui réduit – jusqu’à la neutralisation complète – la production de cette hormone, dont la tâche est de réguler l’utilisation du glucose. par les cellules, entraînant une situation d’excès de glucose dans le sang, appelée hyperglycémie.
Comment fonctionne le teplizumab pour le traitement du diabète de type 1
Le médicament, qui est administré par perfusion intraveineuse une fois par jour pendant 14 jours consécutifs, lie certaines cellules du système immunitaire, retardant la progression de la maladie. « Peut désactiver les cellules immunitaires qui attaquent les cellules productrices d’insuline, tout en augmentant le pourcentage de cellules qui aident à modérer la réponse immunitaire – explique la Food and Drug Administration (FDA) dans une note-. L’approbation d’aujourd’hui d’une thérapie de classe mondiale ajoute une nouvelle option de traitement importante pour certains patients à risque”.
Indiqué pour retarder l’apparition du diabète de type 1 de stade 3 chez les adultes et les patients pédiatriques de 8 ans et plus qui souffrent actuellement de diabète de type 1 de stade 2, le médicament – approuvé aux États-Unis sous le nom de Tzield commercial – a été testé dans une étude clinique, qui a évalué l’innocuité et l’efficacité chez 76 patients atteints de diabète de stade 2 de type 1. Dans l’étude, les patients ont reçu au hasard soit Tzield soit un placebo une fois par jour par perfusion intraveineuse pendant 14 jours.
Les résultats des essais ont montré que sur une moyenne de 51 mois, 45 % des 44 patients ayant reçu Tzield ont développé un diabète de stade 3 de type 1, contre 72 % des 32 patients ayant reçu un placebo. Chez les patients traités par Tzield, le délai médian de diagnostic du diabète de type 1 de stade 3 était de 50 mois contre 25 mois chez les patients ayant reçu un placebo. Les effets secondaires les plus courants du médicament comprenaient une diminution des niveaux de certains globules blancs, des éruptions cutanées et des maux de tête.